摘要:典型的女性性激素雌激素刺激血管細(xì)胞向肌肉輸送胰島素,降低血糖,預(yù)防2型糖尿病。
德克薩斯大學(xué)西南醫(yī)學(xué)中心的研究人員報(bào)告稱,典型的女性性激素雌激素刺激血管細(xì)胞向肌肉輸送胰島素,降低血糖,預(yù)防2型糖尿病。該研究結(jié)果發(fā)表在《自然通訊》雜志上,最終可能會(huì)導(dǎo)致2型糖尿病的新療法,這種疾病影響著全球數(shù)億人,并且越來越普遍。

圖1 ERα通過加強(qiáng)內(nèi)皮胰島素向骨骼肌的轉(zhuǎn)運(yùn)改善葡萄糖耐受
研究負(fù)責(zé)人Philip Shaul博士說,“這項(xiàng)對(duì)小鼠的研究揭示了一種新的機(jī)制,可以增強(qiáng)胰島素向肌肉的輸送,體內(nèi)80%的葡萄糖都在肌肉中被處理掉”。
研究人員早就知道,雌激素似乎可以預(yù)防2型糖尿病,這是一種以高血糖或葡萄糖為特征的疾病,由控制血糖的身體器官中胰島素作用的喪失引起。例如,經(jīng)歷自然更年期或通過手術(shù)切除產(chǎn)生雌激素的卵巢進(jìn)入這種狀態(tài)的女性患2型糖尿病的風(fēng)險(xiǎn)明顯高于絕經(jīng)前女性,而這種風(fēng)險(xiǎn)通常可以通過激素替代療法來降低。同樣,攜帶突變使雌激素受體失活的男性也更有可能患上這種疾病。雌激素受體在細(xì)胞中調(diào)節(jié)雌激素的作用。
盡管雌激素對(duì)肌肉和脂肪組織的代謝作用已被充分記錄,但其對(duì)血管內(nèi)皮細(xì)胞的影響尚不清楚。
為了了解更多信息,Shaul博士和他的同事們研究了一些小鼠,這些小鼠通過遺傳技術(shù)從內(nèi)皮細(xì)胞中選擇性地刪除了雌激素受體。就像攜帶雌激素受體突變的人類一樣,攜帶這種變異的雄性老鼠患上了一種嚙齒動(dòng)物形式的2型糖尿病。在切除卵巢并飼喂高脂肪飲食的雌性小鼠中——這是健康動(dòng)物患2型糖尿病的處方,可以通過雌激素治療逆轉(zhuǎn)——內(nèi)皮細(xì)胞中雌激素受體基因的選擇性沉默導(dǎo)致雌激素的抗糖尿病作用完全喪失。這些實(shí)驗(yàn)表明,在兩性中,雌激素受體在內(nèi)皮細(xì)胞降低血糖中起著關(guān)鍵作用。
在培養(yǎng)細(xì)胞中進(jìn)行的進(jìn)一步實(shí)驗(yàn)表明,當(dāng)雌激素刺激內(nèi)皮細(xì)胞上的雌激素受體時(shí),胰島素很容易從細(xì)胞的一側(cè)轉(zhuǎn)運(yùn)到另一側(cè)。在小鼠身上,這種效應(yīng)導(dǎo)致胰島素從血液流向骨骼肌,消耗了體內(nèi)絕大部分的葡萄糖。進(jìn)一步觀察發(fā)現(xiàn),一種被稱為分類連接蛋白5 (SNX5)的蛋白質(zhì)在這一過程中起著關(guān)鍵作用。研究人員表明,使用基因技術(shù)關(guān)閉內(nèi)皮細(xì)胞中的這種蛋白會(huì)導(dǎo)致雌激素刺激胰島素運(yùn)輸能力的喪失,就像刪除雌激素受體一樣。
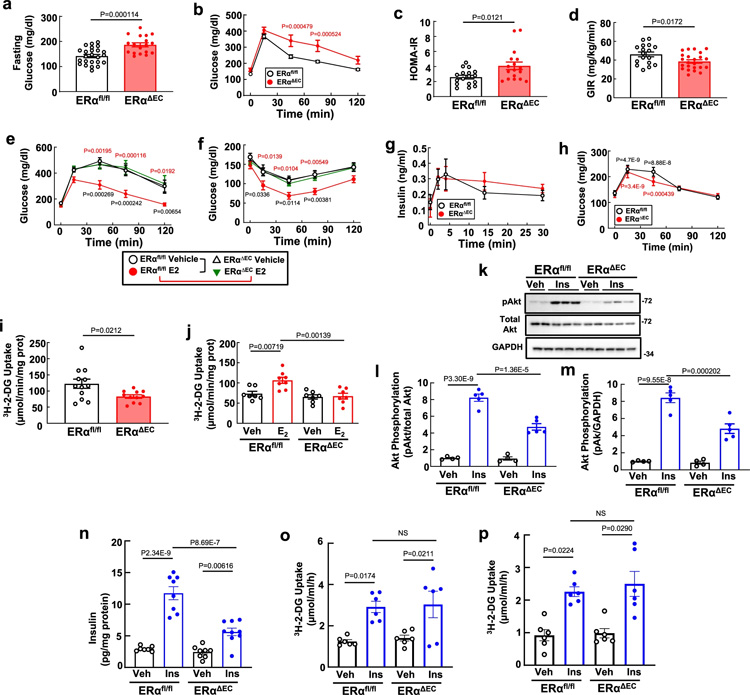
圖2 ERα通過增強(qiáng)胰島素向骨骼肌的輸送來改善葡萄糖耐受和胰島素敏感性
Shaul博士說,這些研究結(jié)果表明,無論是男性還是女性,雌激素對(duì)內(nèi)皮細(xì)胞的作用對(duì)于將胰島素輸送到骨骼肌至關(guān)重要,從而降低血糖。需要進(jìn)一步的工作來確定雌激素促進(jìn)胰島素轉(zhuǎn)運(yùn)到男性肌肉的來源。他說,通過利用有利于內(nèi)皮細(xì)胞胰島素轉(zhuǎn)運(yùn)的機(jī)制,科學(xué)家最終可能能夠開發(fā)出治療2型糖尿病的新療法。
本研究由美國國立衛(wèi)生研究院資助(HL144572, DK110127, HL098040, S10OD021685-01A1, DK015556, CA220284, EB025841和DK126833),乳腺癌研究基金會(huì)資助(BCRF20-083和BCRF20-084),美國心臟協(xié)會(huì)(19POST34390001)和聯(lián)合第一資本公司兒科杰出主席支持。
參考資料
[1] Endothelial ERα promotes glucose tolerance by enhancing endothelial insulin transport to skeletal muscle
摘要:典型的女性性激素雌激素刺激血管細(xì)胞向肌肉輸送胰島素,降低血糖,預(yù)防2型糖尿病。
德克薩斯大學(xué)西南醫(yī)學(xué)中心的研究人員報(bào)告稱,典型的女性性激素雌激素刺激血管細(xì)胞向肌肉輸送胰島素,降低血糖,預(yù)防2型糖尿病。該研究結(jié)果發(fā)表在《自然通訊》雜志上,最終可能會(huì)導(dǎo)致2型糖尿病的新療法,這種疾病影響著全球數(shù)億人,并且越來越普遍。

圖1 ERα通過加強(qiáng)內(nèi)皮胰島素向骨骼肌的轉(zhuǎn)運(yùn)改善葡萄糖耐受
研究負(fù)責(zé)人Philip Shaul博士說,“這項(xiàng)對(duì)小鼠的研究揭示了一種新的機(jī)制,可以增強(qiáng)胰島素向肌肉的輸送,體內(nèi)80%的葡萄糖都在肌肉中被處理掉”。
研究人員早就知道,雌激素似乎可以預(yù)防2型糖尿病,這是一種以高血糖或葡萄糖為特征的疾病,由控制血糖的身體器官中胰島素作用的喪失引起。例如,經(jīng)歷自然更年期或通過手術(shù)切除產(chǎn)生雌激素的卵巢進(jìn)入這種狀態(tài)的女性患2型糖尿病的風(fēng)險(xiǎn)明顯高于絕經(jīng)前女性,而這種風(fēng)險(xiǎn)通??梢酝ㄟ^激素替代療法來降低。同樣,攜帶突變使雌激素受體失活的男性也更有可能患上這種疾病。雌激素受體在細(xì)胞中調(diào)節(jié)雌激素的作用。
盡管雌激素對(duì)肌肉和脂肪組織的代謝作用已被充分記錄,但其對(duì)血管內(nèi)皮細(xì)胞的影響尚不清楚。
為了了解更多信息,Shaul博士和他的同事們研究了一些小鼠,這些小鼠通過遺傳技術(shù)從內(nèi)皮細(xì)胞中選擇性地刪除了雌激素受體。就像攜帶雌激素受體突變的人類一樣,攜帶這種變異的雄性老鼠患上了一種嚙齒動(dòng)物形式的2型糖尿病。在切除卵巢并飼喂高脂肪飲食的雌性小鼠中——這是健康動(dòng)物患2型糖尿病的處方,可以通過雌激素治療逆轉(zhuǎn)——內(nèi)皮細(xì)胞中雌激素受體基因的選擇性沉默導(dǎo)致雌激素的抗糖尿病作用完全喪失。這些實(shí)驗(yàn)表明,在兩性中,雌激素受體在內(nèi)皮細(xì)胞降低血糖中起著關(guān)鍵作用。
在培養(yǎng)細(xì)胞中進(jìn)行的進(jìn)一步實(shí)驗(yàn)表明,當(dāng)雌激素刺激內(nèi)皮細(xì)胞上的雌激素受體時(shí),胰島素很容易從細(xì)胞的一側(cè)轉(zhuǎn)運(yùn)到另一側(cè)。在小鼠身上,這種效應(yīng)導(dǎo)致胰島素從血液流向骨骼肌,消耗了體內(nèi)絕大部分的葡萄糖。進(jìn)一步觀察發(fā)現(xiàn),一種被稱為分類連接蛋白5 (SNX5)的蛋白質(zhì)在這一過程中起著關(guān)鍵作用。研究人員表明,使用基因技術(shù)關(guān)閉內(nèi)皮細(xì)胞中的這種蛋白會(huì)導(dǎo)致雌激素刺激胰島素運(yùn)輸能力的喪失,就像刪除雌激素受體一樣。

圖2 ERα通過增強(qiáng)胰島素向骨骼肌的輸送來改善葡萄糖耐受和胰島素敏感性
Shaul博士說,這些研究結(jié)果表明,無論是男性還是女性,雌激素對(duì)內(nèi)皮細(xì)胞的作用對(duì)于將胰島素輸送到骨骼肌至關(guān)重要,從而降低血糖。需要進(jìn)一步的工作來確定雌激素促進(jìn)胰島素轉(zhuǎn)運(yùn)到男性肌肉的來源。他說,通過利用有利于內(nèi)皮細(xì)胞胰島素轉(zhuǎn)運(yùn)的機(jī)制,科學(xué)家最終可能能夠開發(fā)出治療2型糖尿病的新療法。
本研究由美國國立衛(wèi)生研究院資助(HL144572, DK110127, HL098040, S10OD021685-01A1, DK015556, CA220284, EB025841和DK126833),乳腺癌研究基金會(huì)資助(BCRF20-083和BCRF20-084),美國心臟協(xié)會(huì)(19POST34390001)和聯(lián)合第一資本公司兒科杰出主席支持。
參考資料
[1] Endothelial ERα promotes glucose tolerance by enhancing endothelial insulin transport to skeletal muscle



